
Menschen in Europa leiden an klinisch relevanter TI5

Medikamente können die Symptome behandeln, jedoch nicht die TI selbst, die weiter fortschreiten kann.3,4

Menschen in Europa leiden an klinisch relevanter TI5

der Patient*innen mit leichter oder trivialer TI zeigten innerhalb von ca. 3 Jahren Progridienz zu mittelschwerer bis schwerer TI6‡

der Patient*innen mit schwerer TI versterben schätzungsweise innerhalb eines Jahres nach Diagnose2,7
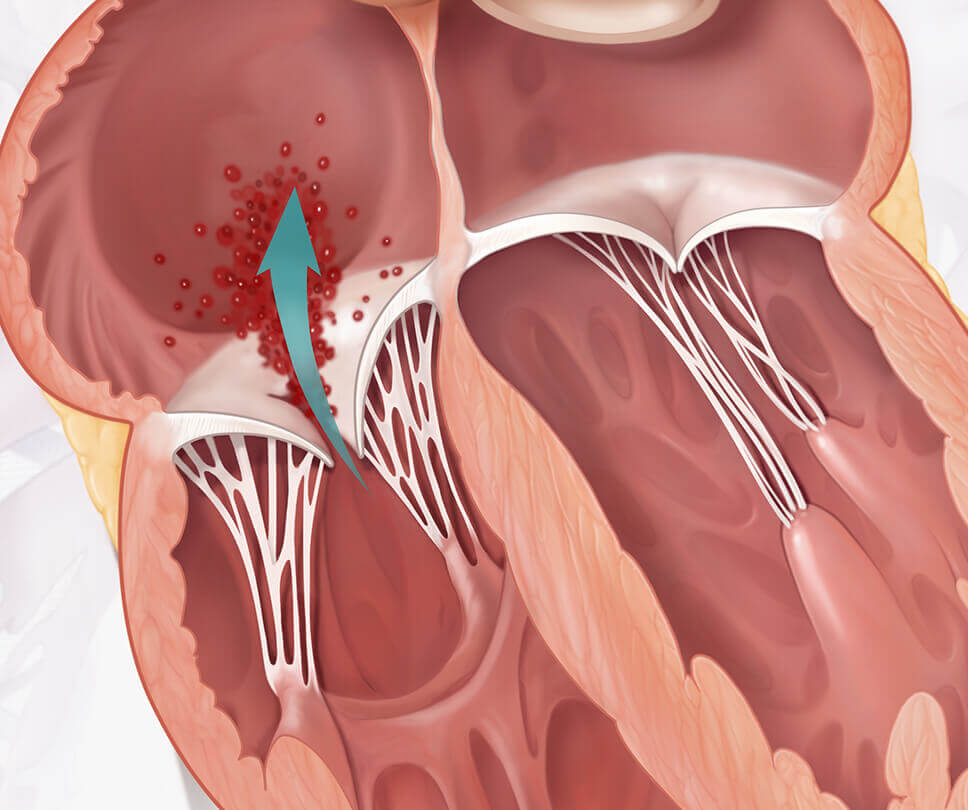
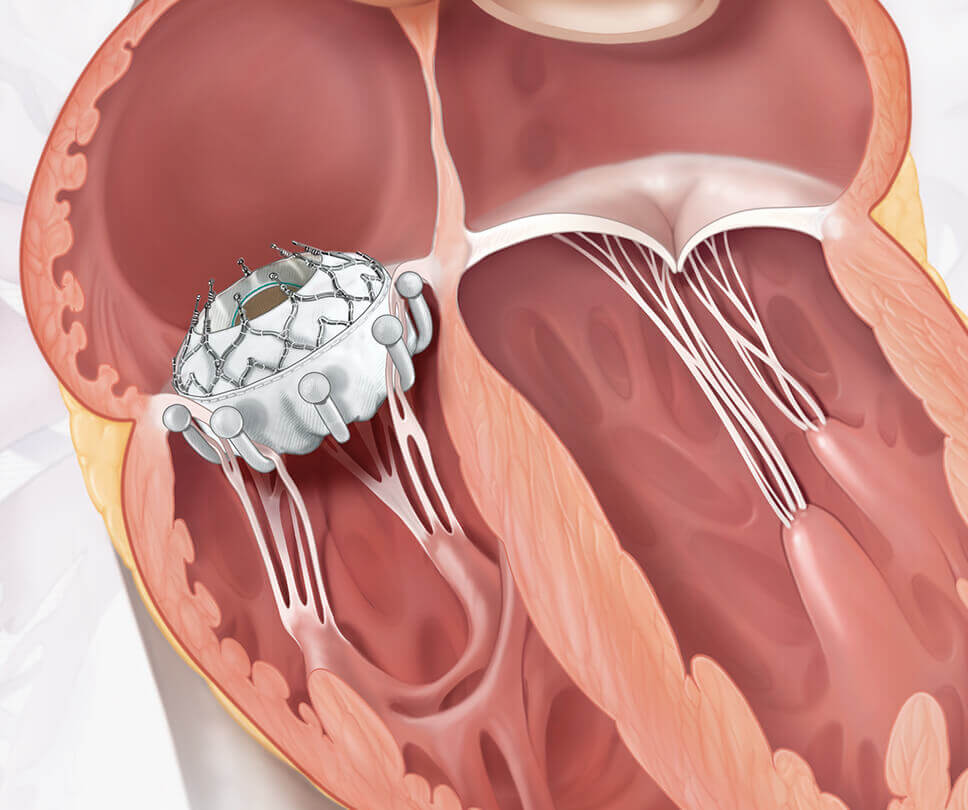
Bewegen Sie den Pfeil nach links oder rechts, um ein Herz mit Trikuspidalklappeninsuffizienz mit einem Herzen mit EVOQUE Klappe zu vergleichen.


Da der TI-Schweregrad fortschreiten kann, kann die Verringerung des TI-Schweregrads die Lebensqualität der Patient*innen verbessern.3,8
* Neuartiges Produkt, das im Handel erhältlich ist (in der EU).
†Auf der Basis von Daten aus den USA.
‡Auf der Basis einer retrospektiven echokardiographischen Analyse von israelischen Patient*innen.
§In einer gepaarten Analyse der ersten 150 Patient*innen der Studie TRISCEND II erreichten 77,8 % der Patient*innen mit EVOQUE+OMT eine vollständige Behebung der TI/Reduzierung auf einen geringfügigen TI-Schweregrad bei der Nachbeobachtung nach 6 Monaten (n = 81).
Die neuartige Option zum Transkatheter-Trikuspidalklappenersatz für infrage kommende Patient*innen*
* Neuartiges Produkt, das im Handel erhältlich ist (in der EU).
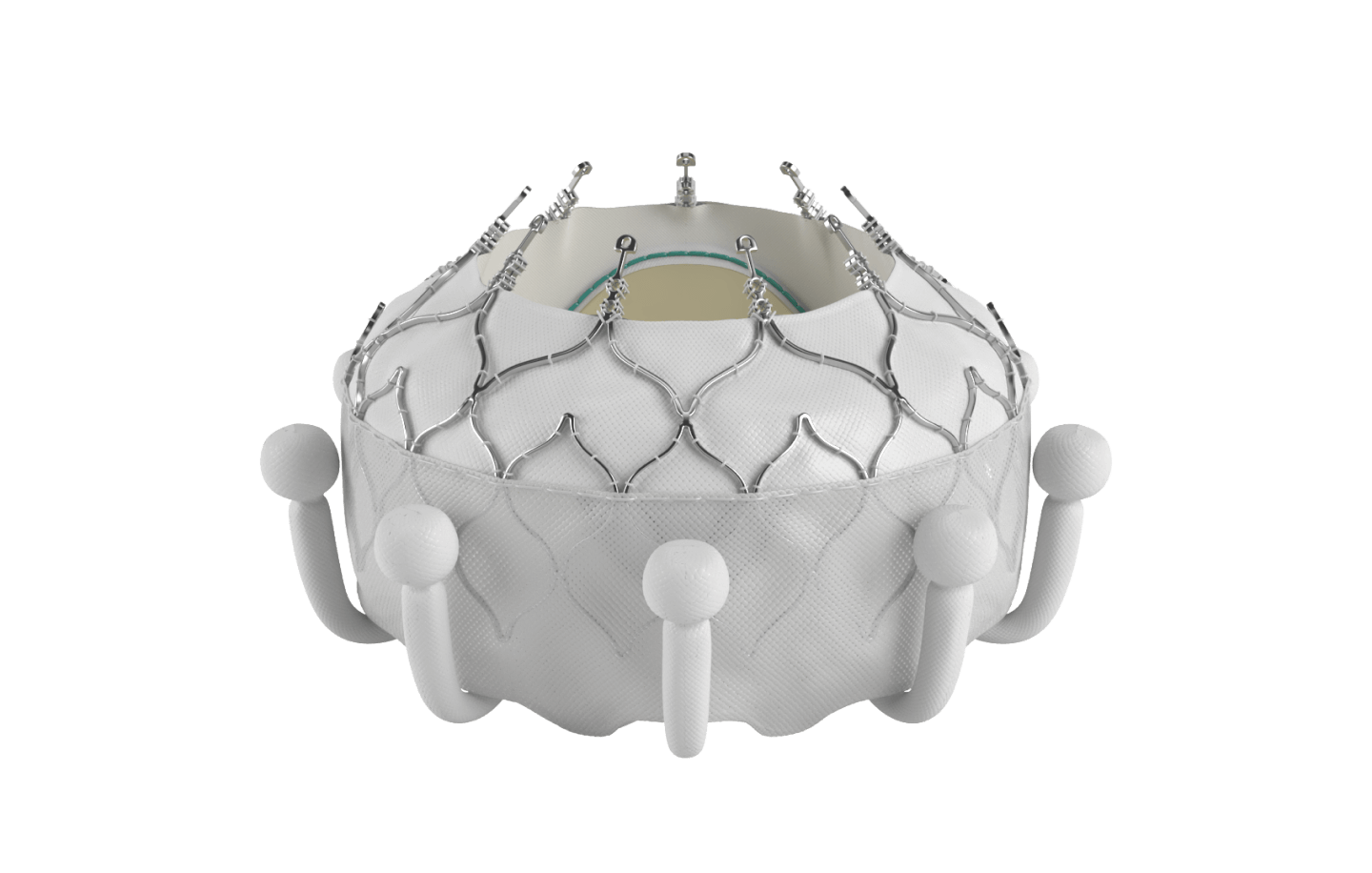
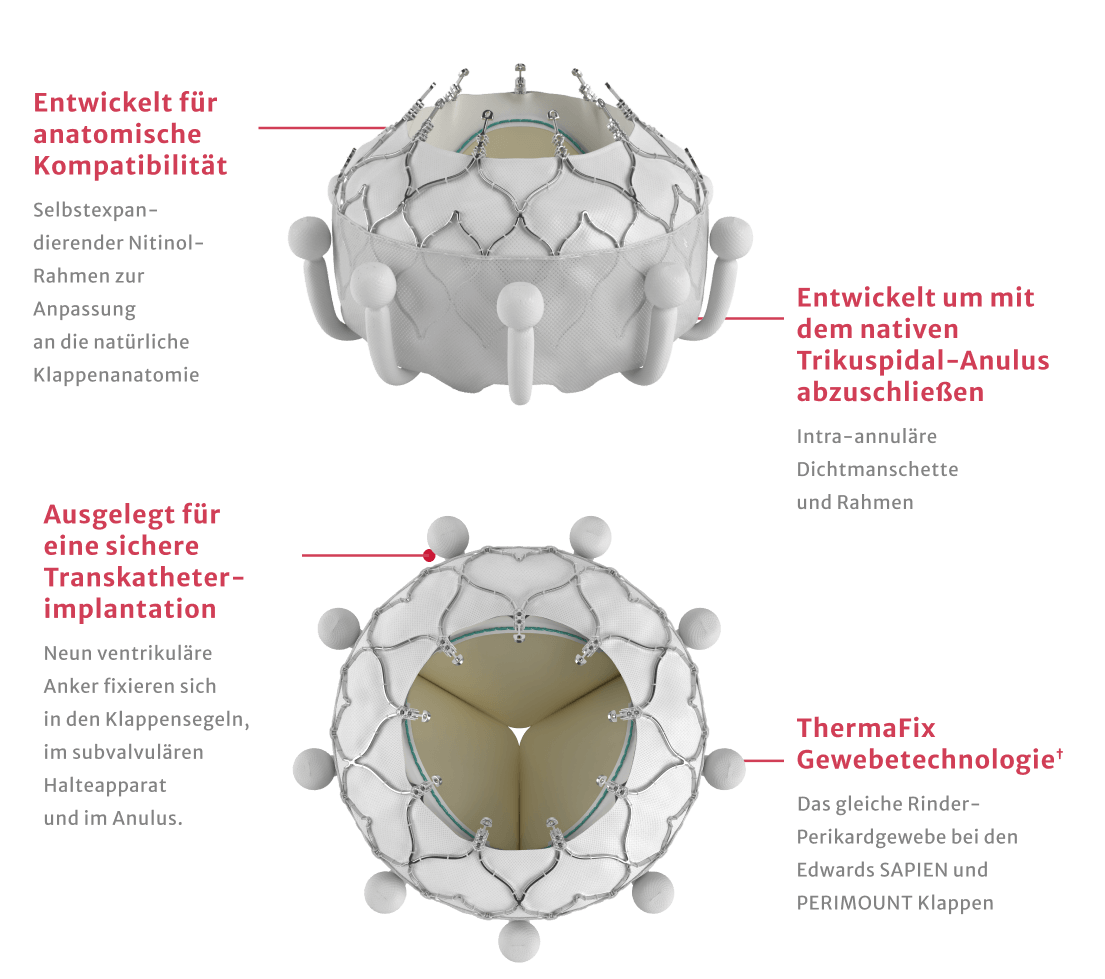
† Es stehen keine klinischen Daten für die Evaluierung der langfristigen Auswirkungen des Carpentier-Edwards ThermaFix Gewebeverfahrens bei Patient*innen zur Verfügung.
‡ Gilt nicht für Edwards SAPIEN 3 Ultra RESILIA Klappen.
Effizientes Verfahren mit einer durchschnittlichen Produktzeit von 65 Minuten*
* Produktzeit ist definiert als die Zeit von der Einführung des Applikationssystems bis zum Entfernen des Applikationssystems.


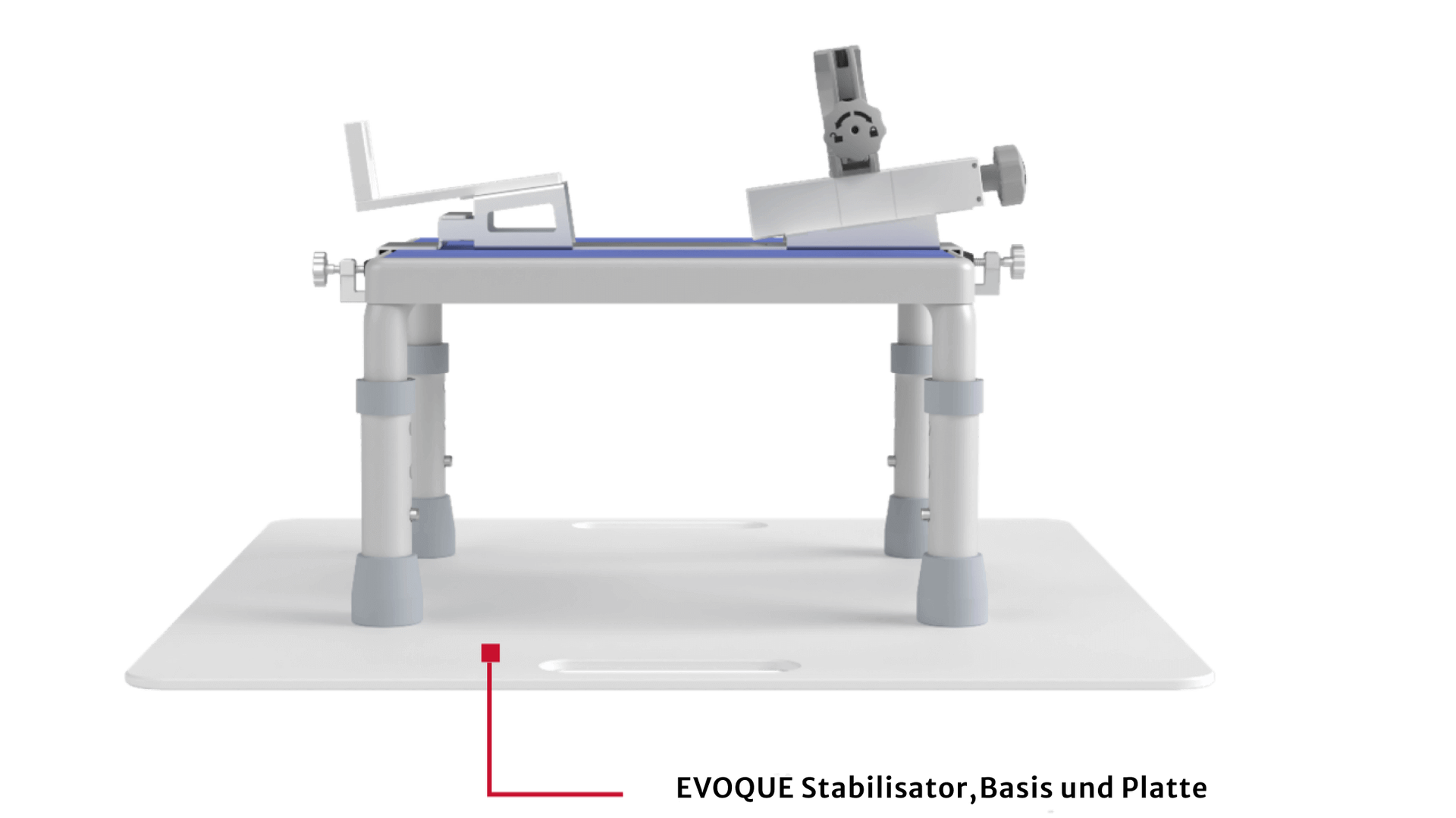
Applikationssystem ist mit flachem Profil und 3 Bewergungsebenen ganz auf die kontrollierte Positionierung ausgelegt
Daten zeigen, dass das EVOQUE System eine TI beheben kann.*
* In einer gepaarten Analyse der ersten 150 Patient*innen der Studie TRISCEND II erreichten 77,8 % der Patient*innen mit EVOQUE+OMT eine vollständige Behebung der TI/Reduzierung auf einen geringfügigen TI-Schweregrad bei der Nachbeobachtung nach 6 Monaten (n = 81).

Die Zulassungsstudie TRISCEND II ist eine prospektive, globale, multizentrische, randomisierte, kontrollierte klinische Studie zur Evaluierung der Sicherheit und Wirksamkeit des EVOQUE Systems in Kombination mit optimaler medizinischer Therapie (EVOQUE+OMT) im Vergleich zu OMT allein bei Patient*innen mit TI, deren Schweregrad mindestens schwerwiegend ist. Diese Daten beziehen sich auf die ersten 150 Patient*innen, die in die Zulassungsstudie TRISCEND II randomisiert und im Rahmen dieser Studie behandelt wurden und deren Nachbeobachtung noch nicht abgeschlossen ist.9
In der Analyse der ersten 150 Patient*innen erreichte die Zulassungsstudie TRISCEND II den ersten ko-primären Wirksamkeitsendpunkt der Reduzierung des TI-Schweregrads auf ≤ mäßig nach 6 Monaten; 77,8 % der Patient*innen erreichten eine vollständige Behebung der TI/Reduzierung auf einen geringfügigen TI-Schweregrad.
der Patient*innen mit EVOQUE+OMT wiesen nach 6 Monaten eine mäßige TI bzw. eine TI mit einem geringeren Schweregrad als mäßig auf.

der Patient*innen mit EVOQUE+OMT wiesen nach 6 Monaten eine mäßige TI bzw. eine TI mit einem geringeren Schweregrad als mäßig auf.
a Gepoolter Z-Test mit Kontinuitätskorrektur zum Vergleich mit dem einseitigen Signifikanzniveau von 0,025.
b Kumulative valvuläre TI-Raten sind im Diagramm oben dargestellt. Mehr als 85 % der Patient*innen der Gruppe mit EVOQUE+OMT wiesen nach 6 Monaten gar kein/ein geringfügiges PVL auf. Ein leichtes PVL wurde für 8,8 % nach 6 Monaten berichtet, während ein mäßiges PVL für 2,5 % nach 6 Monaten gemeldet wurde. Für keine Patient*in wurde ein schweres oder größeres PVL nach 6 Monaten berichtet.
Zu den CEC-beurteilten schwerwiegenden unerwünschten Ereignissen gehören u. a.:
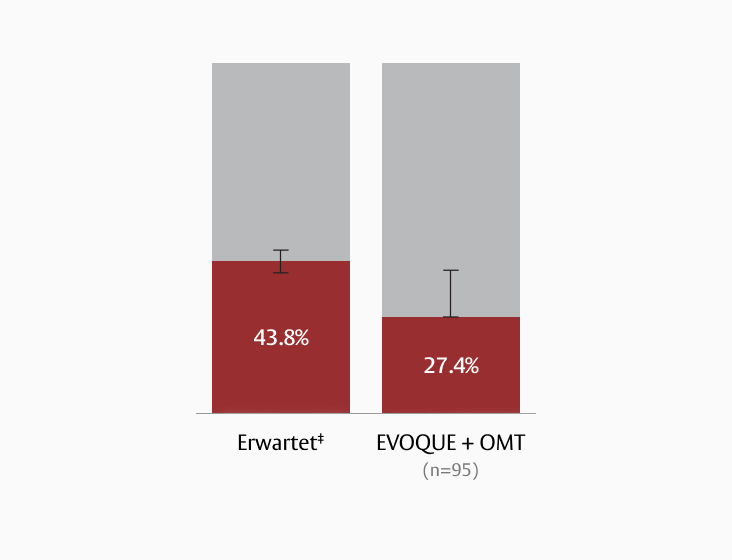
Zu den CEC-beurteilten schwerwiegenden unerwünschten Ereignissen gehören u. a.:
* In einer Analyse der ersten 150 Patient*innen der Zulassungsstudie TRISCEND II wiesen 27,4 % (26/95) der Patient*innen mit EVOQUE+OMT nach 30 Tagen schwere unerwünschte Ereignisse auf.
† Bei den Patient*innen trat mehr als 1 Ereignis auf.
‡ SUEs gemäß Medicare FFS Leistungsansprüchen, Standardanalysedateien aus der Kohorte mit isolierter Operation zum TV-Ersatz 2011–2018, N = 2036.
§ Tödliche, lebensbedrohliche, ausgeprägte oder größere Blutung, definiert gemäß Mitral Valve Academic Research Consortium
93,8 % der Patient*innen, die mit EVOQUE+OMT behandelt wurden, wiesen nach 6 Monaten eine leichte TI bzw. eine TI mit einem geringeren Schweregrad als leicht auf.*
* In einer gepaarten Analyse der ersten 150 Patient*innen der Studie TRISCEND II erhielten Patient*innen EVOQUE+OMT (n = 81).
In der Analyse der ersten 150 Patient*innen erfüllte die Zulassungsstudie TRISCEND II den zweiten ko-primären kombinierten Wirksamkeitsendpunkt, bestehend aus klinisch bedeutsamer Ergebnisse hinsichtlich Funktion und Lebensqualität nach 6 Monaten.

mittlere Verbesserung des zusammenfassenden KCCQ-Gesamtscores im Zeitraum von Baseline bis 6 Monate in der Gruppe mit EVOQUE+OMT.

der Patient*innen der Gruppe mit EVOQUE+OMT erreichten NYHA-Klasse I/II nach 6 Monaten.

Unterschied in Bezug auf das mediane Ergebnis des 6MGT zwischen der Gruppe mit EVOQUE+OMT und der Gruppe nur mit OMT.


Hierarchischer kombinierter Endpunkt

Verbesserung des KCCQ-Scores

Verbesserung der NYHA-Klasse

mittlere Verbesserung des zusammenfassenden KCCQ-Gesamtscores im Zeitraum von Baseline bis 6 Monate in der Gruppe mit EVOQUE+OMT.
der Patient*innen der Gruppe mit EVOQUE+OMT erreichten NYHA-Klasse I/II nach 6 Monaten.
Unterschied in Bezug auf das mediane Ergebnis des 6MGT zwischen der Gruppe mit EVOQUE+OMT und der Gruppe nur mit OMT.
a Die untere Grenze des einseitigen 97,5%-Konfidenzintervalls ist 2,6.
b Die Verbesserung des zusammenfassenden KCCQ-Gesamtscores beträgt ≥ 10 Punkte.
c Die Verbesserung der NYHA-Funktionsklasse beträgt ≥ 1 Klasse.
d Die Verbesserung des 6MGT beträgt ≥ 30 Meter.
Hier finden Sie Antworten auf Ihre Fragen über das EVOQUE System und erfahren mehr über die klinische Evidenz der Zulassungsstudie TRISCEND II.

Für Indikationen, Gegenanzeigen, Vorsichtsmaßnahmen, Warnhinweise und mögliche Nebenwirkungen bitte die Packungsbeilage beachten (ggf. unter eifu.edwards.com abzurufen).